第五单元 化学方程式 课题2 怎么样正确书写化学方程式(讲学)
__________
通过具体化学反应,剖析理解化学方程式的涵义
知道书写化学方程式应遵守的原则
能正确书写简单的化学方程式
__________
____________________
1.书写化学方程式要遵守两个原则:一是需要以__________为基础;二是要遵循__________定律。
2.化学方程式的步骤:①依据实验事实,在式子的左、右两边__________反应物和生成物的化学式,并在式子左、右两边之间画一条短线;②__________化学方程式;③__________化学反应发生的条件,把短线改成__________。
要点1、化学式及其意义
____________________
1、化学方程式的定义:用化学式表示化学反应的式子。
2、意义:
①宏观方面:表明反应物、生成物是什么,反应在哪些条件下发生;
②微观方面:表示反应体系中各物质的微观粒子的数目关系;
③量的方面:表示反应体系中各物质的水平关系。
____________________
1、化学方程式不只可表明反应物、生成物是什么,反应在哪些条件下发生;还可以表示反应体系中各物质的微观粒子的数目关系。如此更能体现出化学反应是遵循水平守恒定律的。
2、化学方程式是在符号表达式基础上,通过在化学式前面加上化学计量数而体现出了反应前后原子的个数不变这一特点。
____________________
【考试试题示例】
1、下列关于S+O2![]() SO2的理解不正确的是
SO2的理解不正确的是
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的水平比是2:1
C.反应前后硫原子、氧原子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为1:1
【答案】B
【分析】考试试题剖析:A选项表示硫与氧气在点燃条件下反应生成二氧化硫,是正确的叙述;B选项,是不对的叙述,依据水平关系可知参加反应的硫与氧气的水平比是1:1;C选项反应前后硫原子、氧原子的个数均不变,依据水平守恒定律是正确的叙述;D选项依据化学方程式的意思知,参加反应的氧气与生成的二氧化硫的分子个数比为1:1,是正确的叙述;故答案选择B。
要点2、化学方程式的书写步骤
____________________
书写化学方程式要根据肯定的步骤进行,防止出现一些错误,如没配平,漏掉反应条件等,其具体步骤可总结为:
写——用化学式正确表示反应物和生成物。
配——在反应物和生成物的化学式前面配上适合的化学计量数,__________
注——在“等号”上方用文字或符号注明必要的反应条件[容易见到的反应条件有:点燃、加热、高温、催化剂、光照、通电等]。
标——注明必要的“↑”和“↓”符号。
检——检查是不是完整,是不是存在遗漏的地方。
巧记速记
左写反应物,右写生成物;写准化学式,化学计量数配平;中间连“![]() ”,条件要注明;生成气体和沉淀,要用箭头来标明。
”,条件要注明;生成气体和沉淀,要用箭头来标明。
____________________
【考试试题示例】
下列化学方程式书写正确的是
A.2NaOH+CuSO4=Cu2↓+NaSO4 B.Ba2+H2SO4=BaSO4↓+HNO3
C.C+2CuO![]() 2Cu+CO2 D.Fe2O3+6HCl=
2Cu+CO2 D.Fe2O3+6HCl=![]() 2FeC12+3H2O
2FeC12+3H2O
【答案】C
【分析】A选项中硫酸钠的化学式是不对的书写;B选项化学方程式没配平;C选项是正确的书写;D选项生成物质为氯化铁,不是氯化亚铁;故答案选择C
要点3、化学方程式的配平
____________________
1、化学方程式的配平是指在化学方程式相应的化学式的前面加上适合的化学计量数,以使化学反应前后原子的个数是相等的。
2、化学计量数可表示反应体系中各物质的微观粒子的数目关系。
____________________
1、在配平化学方程式的过程中,只能在化学式的前面加上适合的化学计量数![]() ,而不可以改动化学式。
,而不可以改动化学式。
2、可能过最小公倍数法、归一法等办法来配平化学方程式。不管用什么办法,都是为了使化学反应前后原子的个数是相等的。
3、最小公倍数法介绍:
①找出在反应式两边各出现过一次的元素且原子个数不相等的原子,或者左右两边原子个数相对较多、变化较大的原子为突破口,求出它们的最小公倍数。
②化学式中含该元素的原子去除最小公倍数所得的商就是该化学式的化学计量数。
如:P+O2——P2O5,式子左侧氧原子的个数为2,右侧氧原子的个数为5,两数的最小公倍数为10。因此,在O2前面配上5,在P2O5前配上2,得到P+5O2——2P2O5式子右侧磷的原子数为4,左侧为1,因此在P的前面配上4。
____________________
【考试试题示例】
在反应:□C2H6+□O2=□CO2+□H2O中,方框中各物质的化学计量数应该对应的是()
A. 2、7、4、6 B. 1、5、1、4 C. 1、7、2、5 D. 2、5、4、5
【答案】A
【分析】本题可借助“定一法”进行配平,把C2H6的化学计量数定为1,则O2、CO2、H2O前面的化学计量数分别为:![]() 、2、3,同时扩大2倍,则C2H6、O2、CO2、H2O前面的化学计量数分别为2、7、4、6。故选A。
、2、3,同时扩大2倍,则C2H6、O2、CO2、H2O前面的化学计量数分别为2、7、4、6。故选A。
__________
1、【2017年山东临沂中考化学考试试题】下列化学方程式书写正确的是
A.2NaOH+CuSO4=Cu2↓+NaSO4 B.Ba2+H2SO4=BaSO4↓+HNO3
C.C+2CuO![]() 2Cu+CO2 D.Fe2O3+6HCl=
2Cu+CO2 D.Fe2O3+6HCl=![]() 2FeC12+3H2O
2FeC12+3H2O
【答案】C
【分析】A选项中硫酸钠的化学式是不对的书写;B选项化学方程式没配平;C选项是正确的书写;D选项生成物质为氯化铁,不是氯化亚铁;故答案选择C
2、【2017年天津中考化学考试试题】写出下列反应的化学方程式。
(1)镁在氧气中燃烧______________;
(2)锌和稀硫酸反应______________;
(3)氢械化钠溶液与稀盐酸混合___________![]() ___。
___。
【答案】(1)2Mg+O2![]() 2MgO;(2)Zn+H2SO4=ZnSO4+H2↑ ;(3)NaOH+HCl=NaC
2MgO;(2)Zn+H2SO4=ZnSO4+H2↑ ;(3)NaOH+HCl=NaC![]() l+H2O
l+H2O
【分析】书写化学方程式的步骤一般有四步:1.依据实验事实,在式子的左、右两边分别写出反应物和生成物的化学式,并在式子的左、右两边之间画一条短线;当反应物或生成物有多种时,中间用加号(即“+”)连接起来.2.配平化学方程式,并检查后,将刚刚画的短线改写成等号(表示式子左、右两边每一种元素原子的总数相等).3.标明化学反应发生的条件(因![]() 为化学反应只有在肯定的条件下才能发生);如点燃、加热(常用“△”号表示)、催化剂、通电等.并且,一般都写在等号的上面,若有两个条件,等号上面写一个下面写一个.4.注明生成物中气体或固体的状况符号(即“↑”、“↓”);一般标注在气体或固体生成物的化学式的右侧.但,假如反应物和生成物中都有气体或固体时,其状况符号就不需要标注了.
为化学反应只有在肯定的条件下才能发生);如点燃、加热(常用“△”号表示)、催化剂、通电等.并且,一般都写在等号的上面,若有两个条件,等号上面写一个下面写一个.4.注明生成物中气体或固体的状况符号(即“↑”、“↓”);一般标注在气体或固体生成物的化学式的右侧.但,假如反应物和生成物中都有气体或固体时,其状况符号就不需要标注了.![]()

A. C+O2![]() CO2 B. 2CO+O2
CO2 B. 2CO+O2![]() 2CO2
2CO2
C. 2H2+O2![]() 2H2O D. CH4+2O2
2H2O D. CH4+2O2![]() CO2+2H2O
CO2+2H2O
【答案】B
【分析】A、该反应反应条件是点燃,但各物质的分子个数比为1:1:1,不是2:1:2,故选项错误;B、该反应反应条件是点燃,各物质的分子个数比为2:1:2,该反应是化合反应;各物质的水平比(28×2):32:(44×2)=7:4:11,故选项正确;C、该反应反应条件是点燃,各物质的分子个数比为2:1:2,该反应是化合反应;但各物质的水平比(2×2):32:(18×2)=1:8:9,故选项错误;D、该反应反应条件是点燃,但该反应的生成物是两种,不是化合反应,故选项错误。故选B。
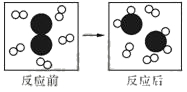
2、下图形象地表示某化学反应前后反应物与生成物分子及其数目的变化,其中![]() 、
、![]() 、
、![]() 分别表示A、B、C三种不一样的分子。则该反应的化学方程式中A、B、C前的化学计量数之比为。
分别表示A、B、C三种不一样的分子。则该反应的化学方程式中A、B、C前的化学计量数之比为。

A.6∶1∶5 B.6∶1∶2 C.2∶1∶2 D.2∶1∶5
【答案】C
【分析】依据水平守恒定律可知参加反应的物质和生成物质的分子个数比为2:1:2,故答案选择C
3、在4Al+3![]() O2
O2![]() 2Al2O3反应中,从分子、原子的角度来看,每______个铝原子和______个氧分子发生反应,生成了______个氧化铝分子;从它们彼此之间的水平比来看,每______份水平的铝和______份水平的氧气反应生成了______份水平的氧化铝。
2Al2O3反应中,从分子、原子的角度来看,每______个铝原子和______个氧分子发生反应,生成了______个氧化铝分子;从它们彼此之间的水平比来看,每______份水平的铝和______份水平的氧气反应生成了______份水平的氧化铝。
【答案】 4 3 2 108 96 204
【分析】化学方程式的意思有三个,它们分别是:(1)表示反应物、生成物和反应条件(可简记为“反、生、条”);(2)表示各物质之间的水平关系(即各物质之间的水平比);(3)表示各物质之间的粒子个数关系(即该物质之间的粒子个数比)。水平关系,可以结合着相对分子水平的计算和化学符号及其周围数字的意义,进行准确地计算。学科~网
解:![]() 参加反应的粒子有铝原子和氧分子,生成物为氧化铝分子,化学方程式的化学计量系数之比即为各物质的粒子的个数之比,所以反应可读作:每 4个铝原子和 3个氧分子发生反应,生成了 2个氧化铝分子;各物质参加反应的水平之比为铝:氧气:氧化铝=(4×27):(3×32):(2×102)=108:96:204。
参加反应的粒子有铝原子和氧分子,生成物为氧化铝分子,化学方程式的化学计量系数之比即为各物质的粒子的个数之比,所以反应可读作:每 4个铝原子和 3个氧分子发生反应,生成了 2个氧化铝分子;各物质参加反应的水平之比为铝:氧气:氧化铝=(4×27):(3×32):(2×102)=108:96:204。







